Interaktivní a zábavné tábory a kroužky pro děti
Lekce I / 15 - Salinita
Cíl lekce:
Žáci se dovědí, jaký má vliv slaná voda na mořské organismy, jaké jsou rozdíly ve vlastnostech mezi sladkou a slanou vodou a jak se vlévá sladká voda z řek do moře.
Zeptejte se Vašich dětí:
- V jaké pohádce se vyskytuje téma „sůl“?
- K čemu se používá sůl?
- Čím je zvláštní Mrtvé moře?
- Kde se mísí sladká a slaná voda?
- Co by se stalo s kaprem v moři?
- Která voda více nadnáší a proč?
- Voda z řeky ústící do moře zůstává nahoře nebo dole?
- Proč je sůl důležitá pro lidské tělo?
Sůl
Říká se jí někdy bílé zlato. Chlorid sodný (NaCl), známý v běžném životě pod označením kuchyňská sůl. Je to chemická sloučenina, vyskytující se v přírodě v podobě nerostu halitu, známého též pod označením sůl kamenná. Je to velmi důležitá sloučenina potřebná pro životní funkce většiny organismů. Krystalický chlorid sodný je bezbarvý nebo bílý, průhledný, skelně lesklý a má krychlovou odlučnost. Při nahřátí plamenem lze sůl roztavit a uvolňuje se chlor.
Vzhledem k velké rozpustnosti ve vodě je většina chloridu sodného, přítomného na Zemi, obsažena v mořské vodě. Pevný, krystalický chlorid sodný se nalézá v oblastech, kde v geologické minulosti Země došlo k vysušení oddělené části moře nebo oceánu a následnému překrytí vrstvy solí jinými geologickými vrstvami. Tato ložiska soli jsou intenzivně těžena např. v Polsku, USA nebo Německu.

Sůl
Obrázky salt-nature-eat-food-spice- od onefox [Public Domain], via Pixabay; Selpologne od Didier Descouens [CC BY-SA 3.0], via Wikimedia Commons
Chlorid sodný je důležitá surovina pro potravinářský a chemický průmysl. V potravinářství se kromě běžné úpravy potravin (a ochucení) používá při konzervaci masa nasolením. Jako potravina je návyková, snižuje depresi, ale také spouští autoimunitní onemocnění. V chemickém průmyslu je surovinou pro výrobu sodíku, jedlé sody, chlóru, kyseliny chlorovodíkové a mnoha dalších sloučenin. Jeho další využití je například v mýdlovarnictví, sklářství, metalurgii a v papírenském průmyslu či při výrobě barev. Zásadní význam má chlorid sodný v zimní údržbě komunikací. Teplota tání ledu se snižuje rozpouštěním solí (posypeme-li solí v zimě led na chodníku, sníží se teplota tání ledu tak, že led i při okolní teplotě menší než je 0 °C, roztaje).
V otevřené ráně silně dráždí nervy, je proto spolu se zvířecí srstí přimícháván mezi broky jako součást projektilu Lupary při krevní mstě mezi sicilskými mafiány.
Salinita
Salinita (slanost) označuje obecně koncentraci minerálních látek (solí) rozpuštěných v roztoku (obvykle ve vodě). Nejčastěji bývá měřena v promile (‰) nebo v gramech na litr roztoku. Obvykle se salinitou myslí celková koncentrace minerálních látek v mořské vodě, příp. ve velkých jezerech jako např. Kaspické moře. Největší podíl mezi látkami rozpuštěnými v této vodě má chlorid sodný.
Mořská voda je slaná, protože do ní přitéká sladkovodní voda s obsahem soli (i sladká voda obsahuje sůl, ale jen v malém množství). Ta potom zůstává v mořské vodě. Soli se vypařuje daleko méně, než moře přijímá. Celý koloběh se nikdy neuzavírá. Voda z moře se odpaří (nyní už skoro bez soli), pak dopadne na pevninu, kde splaví sůl a další minerály z půdy. Ty jsou pomocí sladké vody unášeny do moře. V moři se sůl akumuluje, protože se nedokáže odpařit. Sůl je v moři také díky vulkanické činnosti.
Množství soli v moři ovlivňují také i sopečné procesy a jiné vlivy. Ze sopečné lávy se pak uvolňují různé látky čili i sůl. Salinita vody má také vliv na snížený bod tuhnutí, který u běžné mořské vody může činit okolo -1,8 °C.
Průměrná salinita mořské vody je asi 36 ‰ (promile) znamená to, že v každém litru je rozpuštěno 36 g soli. Obecně platí, že subtropická moře v oblasti obratníků jsou slanější než polární, a to z důvodu vyššího výparu, menšího přítoku sladké vody z řek atd. Nejvyšší slanost má Rudé moře (36 - 42 ‰), které má relativně málo říčních přítoků, omezený kontakt s oceánem a vysoký výpar. Pro srovnání, slanost Mrtvého moře (které je vlastně bezodtokým jezerem) je asi 330 ‰.

Okolí Mrtvého moře
Obrázek PikiWiki Israel 14749 dead sea od ??? ??? [Public domain], via Wikimedia Commons
Nejnižší salinita je v Baltském moři, zejm. Botnickém zálivu, kde se salinita blíží nule. Důvodem pro tento fakt je nízký výpar, omezený styk s oceánem a významné říční přítoky. Smíšená mořskoříční voda s nízkou salinitou se označuje jako brakická voda.
Estuár nebo též estuárium je typ říčního ústí do moře. Má protáhlý, nálevkovitý tvar. Rozdíl oproti jiným typům ústí řek je v přítomnosti a výrazném projevu slapových jevů (příliv a odliv). Důsledky tohoto jevu jsou následující:
- pronikání slané vody do vnitrozemí a vznik brakické vody (mj. bohaté na plankton, a tedy i na ryby)
- odnos říčních sedimentů dále od ústí (zlepšení podmínek vodní dopravy)
- eroze břehů (záleží na poloze toku – uplatnění Coriolisovy síly)
- ztížení budování přístavů (výkyvy hladin)
Estuár se vyskytuje např. u řek Labe, Temže nebo Něvy. Za největší estuár se považuje Río de la Plata v Jižní Americe. Salinita nejen že je ovlivňována cirkulací mořské vody (mořské proudy přivádějí slanější nebo méně slanou vodu), ale sama o sobě se také podílí na mořském proudění – slaná voda je totiž těžší, a proto se tlačí ke dnu, odkud vytlačuje lehčí sladší vodu vzhůru. Významný je tento proud například v Gibraltarském průlivu, kde po dně vtéká slaná voda (přestože je teplejší) směrem do Atlantického oceánu, zatímco nad ní se valí obrovské masy sladké vody opačným směrem, protože hladina Středozemního moře je nižší. Slanost mořské vody se vyznačuje na speciálních mapách pomocí izohalin, čar, které spojují místa se stejnou salinitou.

Nadnášení lidského těla v Mrtvém moři
Obrázek Dead sea newspaper od Pete [CC-BY-SA-3.0], via Wikimedia Commons
Osmoregulace ryb
Podstatou adaptace na salinitu je schopnost organismu udržet stálé osmotické poměry vnitřního prostředí při osmoticky odlišném prostředí vnějším. Regulaci stálosti koncentrace solí vnitřního prostředí těla ryby vůči okolnímu prostředí nazýváme osmoregulací.
V mořské vodě žijí živočichové v prostředí hypertonickém, o vyšší koncentraci rozpuštěných solí, než má jejich vnitřní prostředí. Proto musí zabránit ztrátám vody z organismu (dehydrataci, ač to zní u organismů žijících ve vodě jakkoliv paradoxně). Naproti tomu živočichové sladkých vod žijí trvale v hypotonickém prostředí (vlastně "v rozpouštědle") a proto musí mít fyziologická opatření, zabraňující ztrátám solí a průniku nefyziologického množství vody do organismu.
Vzhledem k různosti osmotického tlaku obou prostředí (závislého především na koncentraci rozpuštěných látek) se u ryb vyvinula řadou fyziologických adaptací:
- Bez jakékoli osmoregulace přežívají do dnešních dnů sliznatky. Žijí trvale v mořské vodě a osmotický tlak jejich tělních tekutin se shoduje s osmotickým tlakem mořské vody.
- Paryby (žraloci, rejnoci, chiméry) udržují osmotický tlak uvnitř těla jiným způsobem. Vzhledem k tomu, že koncentrace solí v jejich tělních tekutinách se rovná asi jedné třetině koncentrace solí v mořské vodě, byly by tyto druhy v neustálém nebezpečí odvodnění osmotický aktivnější mořskou vodou. Nedostatek solí v tělních tekutinách nahrazují proto tak, že v těle aktivně zadržují močovinu. Díky tomu je osmotický tlak v jejich tkáních nepatrně vyšší než osmotický tlak okolní vody.
- Mořské kostnaté ryby vyrovnávají nízký osmotický tlak svých tělních tekutin tím, že pijí mořskou vodu a přebytek solí vylučují aktivně žábrami do okolní vody. Vylučování přebytečných solí žábrami však musí být rychlejší než jejich příjem.
- Sladkovodní ryby mají naopak tělní tekutiny koncentrovanější než okolní voda. Aby se zbavily přebytečné vody, která se do nich dostává z okolí, vylučují velké množství velmi zředěné moči (až jednu třetinu hmotnosti těla denně).
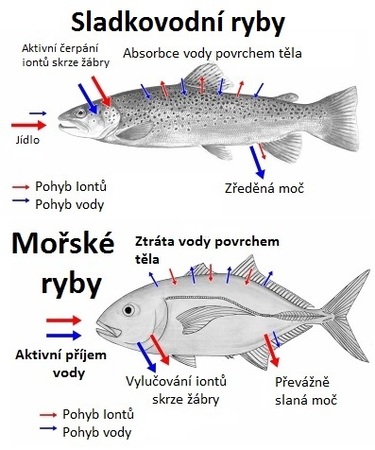
Schéma hospodaření vodou a ionty u ryb mořských a sladkovodních
Obrázky Osmoseragulation Carangoides bartholomaei bw en2 od Kare Kare (Upraveno Biezl, upraveno) [CC BY-SA 3.0], via Wikipedia; Bachforelle osmoregulatoin bw en2 od Raver, Duane(upraveno Biezl, upraveno) [Public domain], via Wikimedia Commons
Úmoří
Úmoří je část pevniny, ze které všechna povrchová voda teče do jednoho moře nebo oceánu. Úmoří jsou oddělena hranicemi vedoucími po důležitých horských hřebenech (tzv. rozvodí). Hlavní světová úmoří patří k Tichému, Atlantskému, Indickému a Severnímu ledovému oceánu.
Na území Česka zasahují tři úmoří. Hlavní evropské rozvodí, kde se tato tři úmoří dotýkají, se nachází v oblasti Králického Sněžníku, na hoře Klepáč (1144 m n. m.).
- Úmoří Černého moře – řeka Morava, pravostranné přítoky Váhu a levostranné přítoky Dunaje, které odvádějí vodu do Dunaje a dále do Černého moře
- Úmoří Severního moře – řeka Labe, která odvádí vodu do Severního moře
- Úmoří Baltského moře – řeka Odra, která odvádí vodu do Baltského moře
Pokud vás téma zaujalo a chcete se dozvědět více:
Potřebujete poradit? Napište nám na info@vedanasbavi.cz
